 |
||
|
 |
||
|
 |
||
|
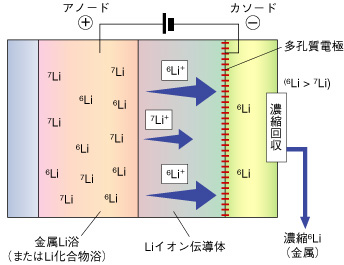
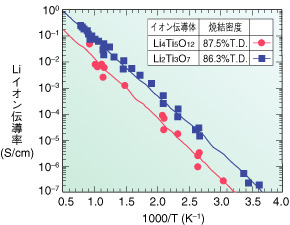
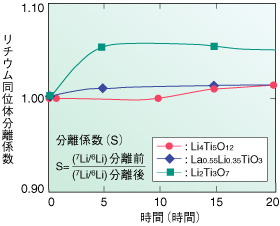
| 核融合炉燃料のトリチウム生産を効率的に行うためには、ブランケット内の6Liの濃度を高くする必要があります。これまで、水銀アマルガム法が、リチウム同位体分離方法に用いられていましたが、水銀による環境汚染などのため、新たなリチウム分離法の開発が望まれています。このため、Liイオン伝導体中で同位体質量の違いによる移動速度の差を利用した同位体分離法(図3-20)を考案し、実証しました。 イオン伝導体として、Liイオン導電率が高いLi2O-TiO2系のスピネル型Li4Ti5O12、ペロブスカイト型La0.55Li0.35TiO3、ラムズデライト型Li2Ti3O7の3種類を選定しました。これら3種類のLiイオン伝導率は10-7~10-1 S/cm(室温~800℃)であり、十分な伝導率を有することを明らかにしました(図3-21)。これらのLiイオン伝導体を用いたリチウム同位体分離効率の測定結果は、スピネル型で1.014、ペロブスカイト型で1.010、ラムズデライト型で1.058であり、水銀アマルガム法のリチウム同位体分離係数(1.02~1.07)と比較して遜色のない値が得られました(図3-22)。実用化に向けた技術開発を進める予定です。 |
| ●参考文献
M. Umeda et al., Preliminary Characterization on Li Isotope Separation with Li Ionic Conductor, Fusion Technol., 39 (2), 654 (2001). |
| ご覧になりたいトピックは左側の目次よりお選びください。 |
|
たゆまざる探究の軌跡-研究活動と成果 2001 Copyright(c) 日本原子力研究所 |