メタンが酸素と1000 ℃付近の高温で、次の式のような部分酸化反応を生じることを利用して、
CH4+1/2O2 → CO+2H2 (1)
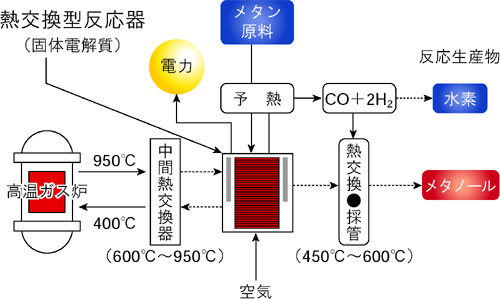
一酸化炭素と水素を作り出すことができます。この反応を燃料電池によって図1-13 のように行うと、燃料電池中の固体電解質膜の片側を酸素イオンが通過すると同時に、この反対側でこの酸素イオンとイオン化の際に放出した電子をメタンに与えることにより、固体電解質膜間で電子の流れを起こせます。また、それと同時に上記(1)式の反応により水素も得ることができます。
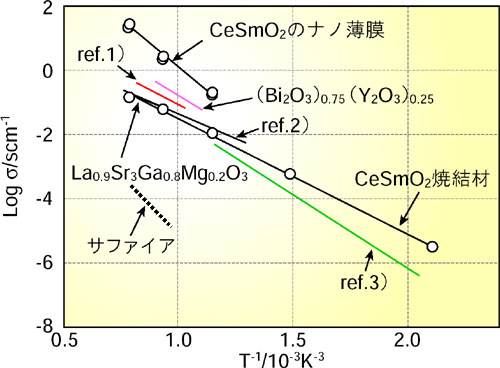
一方、この方法で電力と水素を同時に発生させるためには、1000 ℃付近で高いイオン伝導性を示す固体電解質材料が必要で、図1-14 に1000℃付近で高いイオン伝導率を示すいろいろな固体電解質材料を示します。高温で代表的な材料としてはBiO2系、LaGaO2系ならびにCeO2系の固体電解質が有名です。現在までのところ、BiO2系の固体電解質が最もイオン伝導率の高い材料であったのですが、この材料は融点が低く高温で不安定である弱点があります。そこで、図中2番目に高いイオン伝導率を示すサマリウムを加えて高イオン伝導化したCeSmO2固体電解質を有機溶媒を使ってゾル-ゲル法で化学合成しました。さらに合成後、ゲル化し始め粘性を持った溶液を一定速度で回転させたサファイア単結晶基盤上に滴下して、基盤上で薄いCeSmO2のゲル化膜を形成させて、その後この単結晶を高温で加熱して、ゲル化膜を焼結させたものを図1-15 に示します。サファイア基盤(図中下部)上に数nmのCeSmO2の粒子と、これらの粒子が焼結してできた約250nm 厚みのナノ薄膜が形成していることが分かります。このナノ薄膜のイオン伝導率を1000℃の温度で計測すると、図1-14 に示すような従来の材料より一桁高い極イオン伝導率を示すことが分かりました。この値は、世界最高記録です。
将来、このナノ薄膜を使うことによって、図1-13 に示す電力と水素を同時に生産できる新しいエネルギーシステムができることでしょう。 |