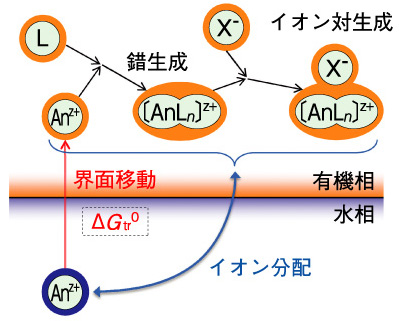
図7-16 水相/有機相界面イオン移動反応
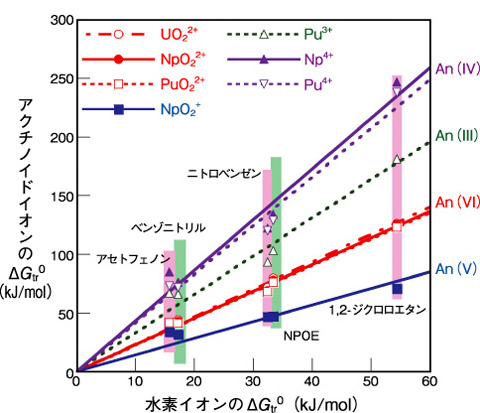
図7-17 アクチノイドと水素イオンのΔGtr0の比較
水と油のような混じり合わない二つの溶液相界面を移動するイオンの移動性は、両溶液相中でのイオンの安定性によって決まるイオン固有のものです。使用済核燃料の再処理で用いられているPUREX法のような溶媒抽出によるイオン分離や、液膜型イオン選択性電極によるイオンの選択的定量は、この移動性の差を利用しています。一般に金属イオンは親水性が高く、有機溶媒に溶け難い性質を持つため、水相から有機相への移動には大きなエネルギー(標準イオン移動ギブズエネルギー:ΔGtr0)が必要です。溶媒抽出では、有機相に移動するイオンを抽出剤(配位子)との錯生成や対イオンとのイオン対生成により安定化させて抽出します(図7-16)。このように、イオンの分配は、錯生成やイオン対生成だけでなく、目的イオンや対イオンのΔGtr0によって決まります。
私たちは、親水性の高いアクチノイドイオンの水/有機相界面でのΔGtr0を精度良く評価するために、まず水素イオンを基準イオンとして選択し、電気化学的な手法により水素イオンのΔGtr0を求めました。次に、水相及び有機相に分配させたアクチノイドと水素イオンの濃度比を正確に測定することにより、3価から6価のU,Np,PuのΔGtr0を決定しました。
五種類の有機溶媒について求めたアクチノイドイオンのΔGtr0を、水素イオンのそれに対してプロットしたものが図7-17です。いずれの有機溶媒を用いた場合でも、アクチノイドイオンのΔGtr0は原子価が同じであれば元素によらずほぼ同じ値をとりました。6価アクチノイドイオンは、これまでΔGtr0が報告されているイオンの中では最も親水性が高いMg2+よりも更に親水的であることが分かりました。イオンの電荷が小さくなるに従い、4価,3価,6価,5価の順にΔGtr0が小さくなりますが、電荷あたりのΔGtr0を比較すると、5価イオンのNpO2+が他のイオンと比べてとりわけ親水性が高いことも分かりました。NpO2+は溶媒抽出が困難なイオンとして知られていますが、NpO2+の親水性が極めて高いことも高い分配比が得られない要因だと考えられます。
本研究では、比較的誘電率の高い有機溶媒を対象としてΔGtr0を決定しましたが、より高感度な分析法を適用できれば、多様な有機溶媒についてΔGtr0を決定でき、分配比の予測による抽出法の開発も期待できます。