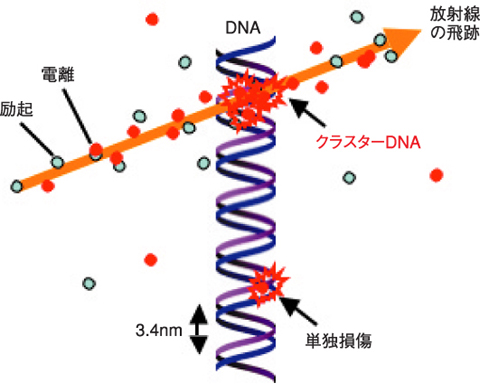
図6-10 放射線によるDNA損傷
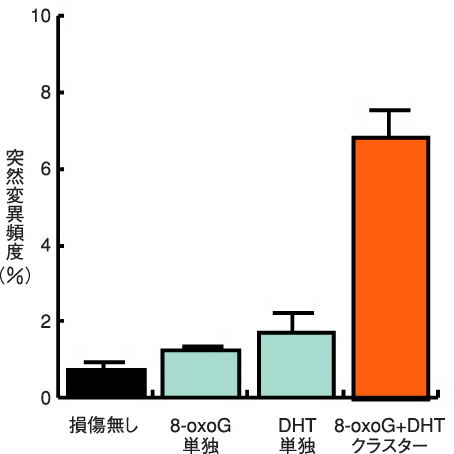
図6-11 クラスターDNA損傷による誘発突然変異頻度
電離放射線は致死や突然変異誘発,発がんなどを引き起こすことが知られています。これら放射線の生物学的効果は、DNAに様々な化学変化(DNA損傷)が生じることが原因と考えられています。放射線によって誘発されるDNA損傷には、DNAの塩基が傷ついた「塩基損傷」やDNAのらせんが切れた「DNA鎖切断」などがあります。一方で、いくつかの化学薬剤も上記のような放射線と同種類のDNA損傷を生じさせることが古くから知られています。しかしながら、化学薬剤により同程度の数の損傷を生じさせても放射線ほど生物学的効果は高くないことが指摘されていました。
この一見矛盾した結果を説明するために、近年「クラスターDNA損傷仮説」が提唱されています。クラスターDNA損傷とはDNA損傷が数nm以内に近接して複数個生じたタイプの損傷です(図6-10)。この説では、「放射線は局所的な電離や励起を引き起こすため、クラスターDNA損傷を誘起する場合があり、そのクラスターDNA損傷の難修復性のため生物効果が高くなる」と仮定しています。
放射線がクラスターDNA損傷を誘起しうることに関しては、これまでそれを示唆する実験結果が集められてきましたが、生じたクラスターDNA損傷が高い生物効果の原因であるという証明は長らくできませんでした。その理由は、放射線照射ではDNA分子上に損傷が様々な種類や個数・ランダムな位置で生じ、クラスター化の効果を生物効果に実験的に対応づけるのが難しいという問題点があったからです。私たちはこれを克服するため、人工的に合成した複数の近接した塩基損傷からなるモデルクラスター損傷を用いて、突然変異誘発を調べる細胞内実験系を考案し開発しました。この方法により、決まった種類,数,位置の損傷の生物効果を調べることが初めて可能となりました。実験を行った結果、8-オキソグアニン(8-oxoG)とジヒドロチミン(DHT)という塩基損傷から構成されるクラスターDNA損傷が高い変異誘発効果を持つことを明らかにし(図6-11)、近接した塩基損傷が突然変異誘発性を増大させることを実験的に示しました。この結果は、「クラスターDNA損傷仮説」の正当性を裏付けるものであり、放射線のリスク評価,がんの放射線治療,放射線突然変異育種など放射線の生物学的応用分野の重要な基礎的知見になると考えられます。