
図7-10 米国核医学会から出版された放射性核種データ集
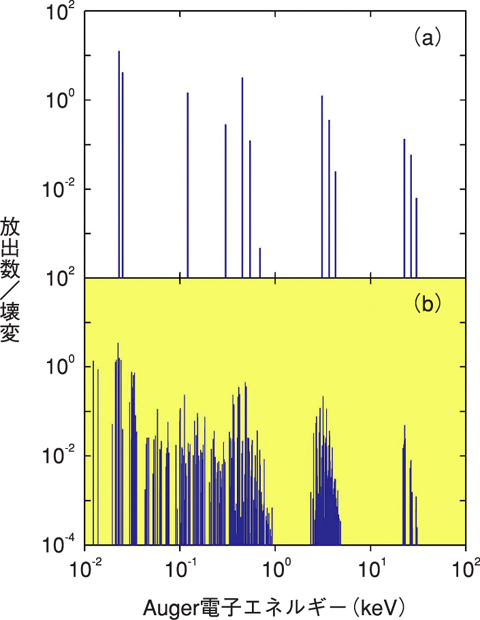
図7-11 125Iから放出されるAuger電子のエネルギー分布の高分解能化
99mTc,123I,67Gaなどで標識した放射性医薬品を投与し、様々な臓器の機能検査、病気の治療を行う核医学検査・治療は、患者の苦痛が少ない方法として世界的に広く利用されています。これらの検査や治療では、投与される放射性医薬品によって患者が受ける被ばく線量を評価し、安全性を確認しながら効果的な結果が得られるように検査・治療計画が立てられます。私たちは、核医学研究で世界をリードする米国核医学会Medical Internal Radiation Dose(MIRD)委員会と協力し、核医学検査に伴う患者の被ばく線量評価に用いる放射性核種データ集“MIRD: Radionuclide Data and Decay Schemes”(1989年発行)を改訂し、その第2版を完成させました(図7-10)。
今回出版された第2版では、これまで課題とされていた放射性医薬品から放出されるAuger電子に対して、詳細な線量計算に必要とされるデータの充実が図られました。放射性医薬品には、軌道電子捕獲や内部転換によって、eV〜keVのAuger電子を多数放出するものがあります。これらのAuger電子は、人体内でnm〜μmの非常に小さな領域に全てのエネルギーを与えるため、DNAの損傷を引き起こし生物学的効果が高いことが知られていました。そこで私たちは、放射性医薬品の投与に伴うDNA損傷の評価を可能にするために、軌道電子捕獲、内部転換に続いて放出されるAuger電子のエネルギーを計算するコードEDISTR04を開発し、すべての放射性医薬品に対し、Auger電子の詳細データを計算する手法を確立しました(図7-11)。この手法を用いて、第1版に収録された242核種に加え、核医学分野の新たな核種の利用に対するニーズに応えるために91核種を追加し、333核種について最新の放射性核種データを収録したデータベースを完成させました。
米国核医学会が開発した線量評価法やデータは、核医学分野の準世界標準的手法として利用されています。今回開発されたデータベースも、核医学診断時の線量評価に利用され、検査及び治療計画の立案や改善、また、新たな検査法の研究にも役立てられます。