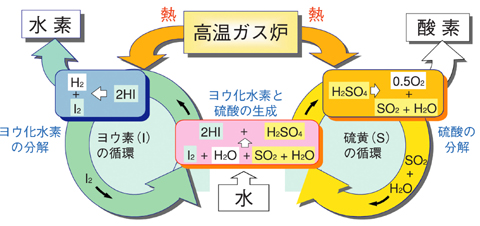
図7-19 ISプロセスの概要
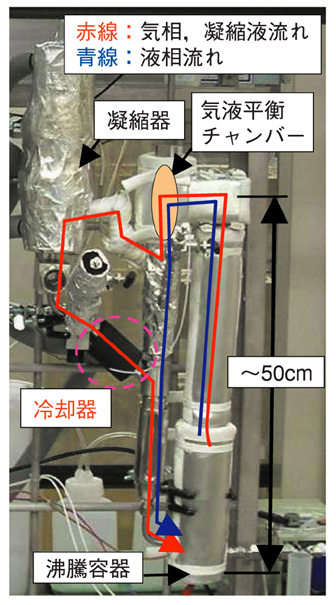
図7-20 循環型平衡蒸留器
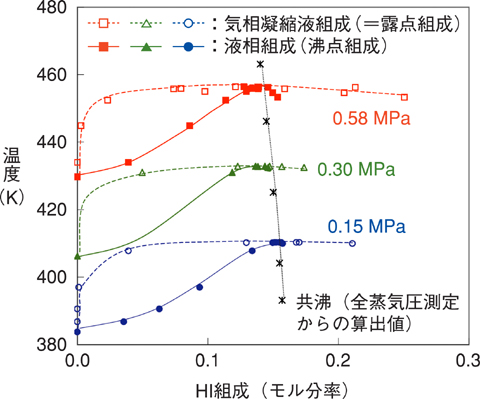
図7-21 HI+H2Oの定圧気液平衡
私たちは、高温ガス炉からの900℃以上の高温の熱を用い、水を原料に大量の水素を安定に製造できる熱化学水素製造法ISプロセスの研究開発を行っています。ISプロセスは、ヨウ素(I)と硫黄(S)を循環物質とする熱化学反応サイクルで、炭酸ガスを発生させずに水素を製造します。現在、高効率で水を水素に変換することが重要な課題のひとつです。
ISプロセスでは、図7-19のように、原料の水(H2O)をヨウ素(I2)及び二酸化硫黄(SO2)と反応させてヨウ化水素(HI)と硫酸(H2SO4)を作り、それらを熱分解して水素と酸素を製造します。HIを熱分解する際に、HI+I2+H2O混合物からHIを蒸留して分離しますが、この蒸留操作がISプロセスの効率に大きな影響を与えます。解析評価を行い、効率的にHIを蒸留するには操作圧力を大気圧以上に高める方が有効であるとの見通しを得ました。しかし、どの程度まで圧力を高めるべきかを評価するには、高圧の気液平衡データが必要で、それらは十分には整備されていませんでした。
そこで、まず、HI+H2O系の高圧の気液平衡データを整備するため、腐食性の強いHI+H2O混合物に耐える測定装置材料を腐食試験を行って選定しました。次に、平衡測定に用いる循環型平衡蒸留器の改良、特に、気相凝縮液を液相と合流させる過程で、HIの沸点が低いことにより合流点付近で液相の熱を受けて凝縮液が再蒸発して逆流する課題を解決するために、気相凝縮液の流路を冷却するなどの工夫,改良を行い、図7-20に示す改良型平衡蒸留器を製作しました。
この装置により、図7-21のように、平衡状態での気相及び液相組成のデータを取得することができました。HI+H2O混合物は気液相が同一組成となる共沸という現象があり、共沸点が全蒸気圧測定結果をもとにした推算値と良く一致していることから、この装置で取得したデータの信頼性が確認されました。また、液相,気相組成のデータを詳細に取得でき、これらの結果により、蒸留装置の設計において過大な尤度を与えなくてもよくなりました。
今後、HI+I2+H2O混合物を含めて、高圧気液平衡に関するデータを充実させて、蒸留装置のコンパクト化と、プロセス効率の向上と蒸留操作圧力の関係を評価し、最適な圧力範囲を決定する予定です。