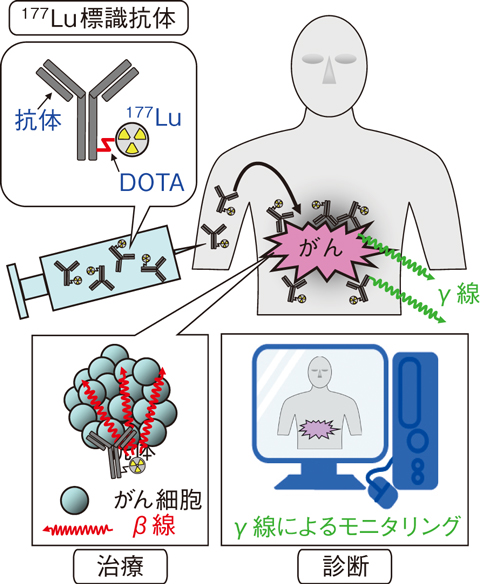
恾5-29丂177Lu昗幆峈懱偵傛傞偑傫偺帯椕媦傃恌抐
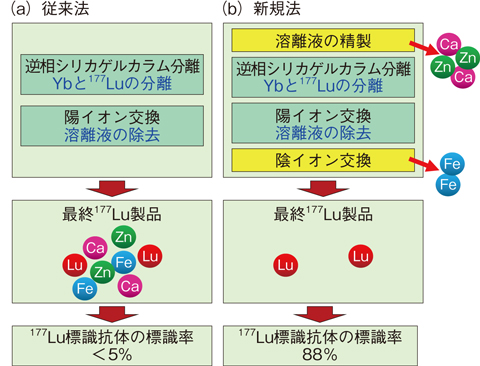
恾5-30丂拞惈巕傪徠幩偟偨Yb偐傜偺177Lu偺暘棧朄
尰嵼丄兝慄傪曻弌偡傞妀庬偑丄偑傫偺帯椕偵梡偄傜傟偰偄傑偡偑丄怴偨側帯椕梡妀庬偲偟偰儖僥僠僂儉177乮177Lu乯偑桳朷帇偝傟偰偄傑偡丅偙傟偼丄177Lu偑兝慄偩偗偱側偔丄懱奜偐傜専弌偡傞偺偵揔偟偨兞慄傪曻弌偡傞摿挜傪旛偊偰偍傝丄帯椕拞偺177Lu偺暘晍傪挷傋偰恌抐偵傕棙梡偱偒傞偲峫偊傜傟傞偨傔偱偡乮恾5-29乯丅
恾5-29偺傛偆偵偑傫嵶朎偵摿堎揑側峈懱偵丄177Lu傪寢崌偟偨177Lu昗幆峈懱傪梡偄偰丄177Lu傪偑傫傑偱撏偗傞帯椕傪曻幩柶塽椕朄偲偄偄傑偡丅偙偺帯椕朄偱偼丄偑傫嵶朎偵敪尰偟偰偄傞峈尨傪棅傝偵峈懱偑177Lu傪塣傃傑偡丅偙偺偲偒丄儖僥僠僂儉摨埵懱拞偺177Lu偺弮搙偑掅偄偲丄偑傫偵撏偔177Lu偑尭偭偰偟傑偄丄帯椕岠壥偑掅壓偟傑偡丅弮搙偺崅偄177Lu偺惗惉偵偼丄拞惈巕敪惗検偺崅偄尨巕楩偱儖僥僠僂儉偺埨掕摨埵懱乮176Lu乯偵拞惈巕傪徠幩偟丄176Lu乮n, 兞乯177Lu斀墳偱捈愙177Lu傪摼傞曽朄偲丄僀僢僥儖價僂儉偺埨掕摨埵懱乮176Yb乯偵拞惈巕傪徠幩偟丄176Yb乮n, 兞乯177Yb乮敿尭婜1.91帪娫乯仺 177Lu斀墳偱惗惉偟偨177Lu傪暘棧偟偰娫愙揑偵摼傞曽朄偺擇偮偑偁傝傑偡丅176Lu偐傜177Lu傪惗惉偝偣傞捈愙朄偼丄墷暷偺偛偔堦晹偺抧堟偵偁傞拞惈巕敪惗検偺崅偄尋媶梡尨巕楩偱偟偐棙梡偱偒傑偣傫偑丄娫愙朄偼丄奺崙偑曐桳偡傞拞惈巕敪惗検偑掅偄尨巕楩偱傕棙梡壜擻偱偡丅偦偙偱丄娫愙朄傪棙梡偟偰儖僥僠僂儉摨埵懱傪娷傑側偄177Lu傪偮偔傞偨傔丄Yb偐傜177Lu傪壔妛揑偵暘棧偡傞條乆側曽朄偑奺崙偱専摙偝傟偰偄傑偡丅
偙傟傑偱偵巹偨偪偼丄媡憡僔儕僇僎儖僇儔儉傪梡偄偰Yb偲177Lu傪姰慡偵暘棧偱偒傞曽朄傪奐敪偟傑偟偨乮恾5-30乮a乯乯丅偟偐偟丄摼傜傟偨177Lu傪梡偄偰177Lu昗幆峈懱傪嶌惢偟偨偲偙傠丄巊梡偟偨177Lu偵懳偟偰177Lu昗幆峈懱偲偟偰摼傜傟偨偺偼5%偵傕枮偨側偄傕偺偱偟偨丅偦偺尨場傪扵偭偨偲偙傠丄巊梡偟偨177Lu梟塼偺拞偵懡検偺僇儖僔僂儉乮Ca乯丆揝乮Fe乯丆垷墧乮Zn乯偑懚嵼偡傞偙偲偑尦慺暘愅偱妋擣偝傟丄偙傟傜偑177Lu偲1,4,7,10-僥僩儔傾僓僔僋儘僪僨僇儞-1,4,7,10-僥僩儔恷巁乮DOTA乯偲偺嶖宍惉傪嫞崌揑偵慾奞偟偨偨傔丄177Lu偺昗幆棪偑掅壓偟偨偙偲傪撍偒巭傔傑偟偨丅傑偨丄偙傟傜偺Ca丆Fe丆Zn偼丄媡憡僔儕僇僎儖僇儔儉暘棧偵梡偄傞2-僸僪儘僉僔僀僜棌巁乮2-HIBA乯媦傃1-僆僋僞儞僗儖儂儞巁僫僩儕僂儉乮1-OS乯帋栻偺晄弮暔偲偟偰娷傑傟偰偄偨偙偲偑暘偐傝傑偟偨丅偦偙偱丄偁傜偐偠傔梲僀僆儞岎姺僇儔儉媦傃僉儗乕僩岎姺僇儔儉偱惛惢偡傞偲偲傕偵丄嵟廔惛惢憖嶌偲偟偰堿僀僆儞岎姺憖嶌傪捛壛偟傑偟偨乮恾5-30乮b乯乯丅偦偺寢壥丄177Lu梟塼拞偺Ca丆Fe丆Zn偺擹搙傪87丆340丆77 ppb偐傜13丆18丆9 ppb偵掅尭偟丄177Lu昗幆峈懱偺昗幆棪傪88%偵忋徃偟偨偙偲偱丄偮偄偵曻幩柶塽椕朄偵梡偄傞偙偲偑偱偒傞崅弮搙偺177Lu偺惢憿偵惉岟偟傑偟偨丅
崱夞巹偨偪偑奐敪偟偨惢憿朄偵傛偭偰丄悽奅奺抧偱崅弮搙177Lu惢昳偺惢憿偑壜擻偲側傟偽丄崱屻177Lu傪梡偄偨曻幩柶塽椕朄偑峀偔晛媦偡傞偙偲偑婜懸偱偒傑偡丅