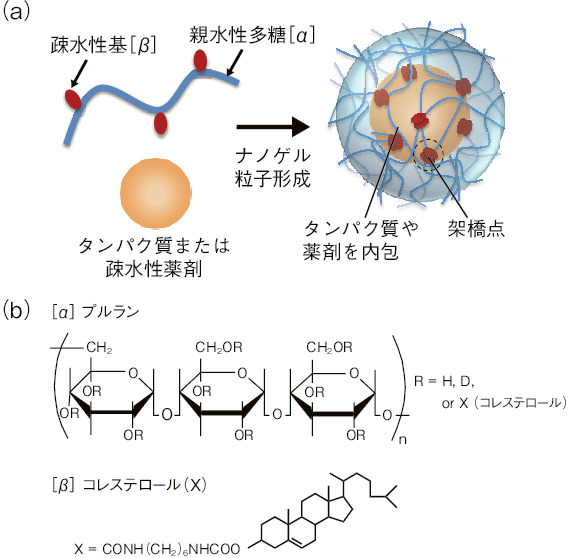
図5-13 ナノゲル微粒子の形成
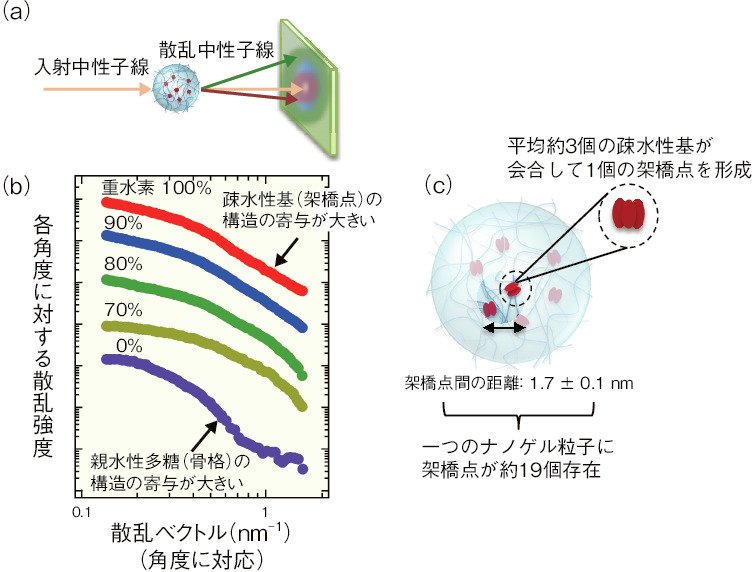
図5-14 小角中性子散乱の概略と結果
図5-13に示すように、疎水性基であるコレステロールを化学的に修飾した天然多糖(プルラン)は疎水性基同士の可逆的な相互作用により水中で自己会合して約30 nmのハイドロゲルナノ粒子(ナノゲル)を形成します。この粒子は体積の90%以上が水から構成されるため、内部にナノスケールの空間を有します。この空間にタンパク質や水に溶けにくい疎水性の薬剤を安定に取り込むことが可能であるため、体内に薬剤等を輸送するドラッグデリバリー(DDS)キャリアとしての応用が期待されています。様々な薬剤のナノゲルへの取り込みや放出はコレステロール基の分布や構造が関与することが知られていますが、水を含むナノサイズの粒子を評価できる手法はほぼ皆無であることから今までその構造は明らかにされていませんでした。そこで、ナノサイズの粒子の構造を調べるのに適した小角中性子散乱(SANS)法を用いて、その内部構造を解明することを試みました。
SANS法は、図5-14(a)に示すように対象物質に中性子線を照射して、その物質による散乱を観察して解析することで1 nmから数µmの構造情報を得る手法です。中性子線は優れた物質透過能力だけでなく、同位体を識別する能力を有するため、対象物の内部の微細構造を非破壊で部分的に明らかにすることが可能です。例えば、多成分から構成される物質中の水素原子(H)を同位体である重水素(D)で部分的に置換することにより散乱にコントラストが付き、各成分の構造情報を検出することができます。
本研究では、溶媒に重水素を加えてプルランに含まれる水酸基(-OH)のHをDに置換することにより、ナノゲル内部のプルラン、コレステロール及び溶媒にコントラストを付与しました。図5-14(b)は溶媒中の重水素の体積比率を0から100%まで変化させた場合のナノゲルの散乱スペクトルを示します。スペクトルの形状はナノゲルの内部の情報を反映しています。図のように、重水素置換によりプルラン、コレステロール、溶媒の散乱コントラストが変化して、スペクトルの形状に変化が観察されました。特異値解析を行うことにより、この強度差からプルラン及びコレステロールの構造情報を含む散乱スペクトルを抽出しました。それらのスペクトルに対してフィッティング解析を行い、各々の大きさや分布を評価した結果、ナノゲルの内部では平均約3個の疎水性基が会合して1個の架橋点を形成しており、全体として19個の架橋点が1.7±0.1 nmの距離で分布して存在していることを明らかにしました。今回初めて得られた知見は、今後、さらなる高性能なDDSキャリア材料を開発する上で重要な情報となります。
中性子を用いた実験はJ-PARCの大強度中性子小角・広角散乱装置「大観」にて行いました。本研究は、日本学術振興会科学研究費補助金若手研究(B)(No.25790087)「中性子ビームを用いた新規ナノゲル材料の開発」の助成を受けたものです。