![図4-4 推定される[NiFe]ヒドロゲナーゼ活性中心の構造](img/honbun/j2008_4-4.jpg)
図4-4 推定される[NiFe]ヒドロゲナーゼ活性中心の構造
![図4-5 [NiFe]ヒドロゲナーゼモデル化合物の酵素類似反応](img/honbun/j2008_4-5.jpg)
図4-5 [NiFe]ヒドロゲナーゼモデル化合物の酵素類似反応
水素分子を活性化させる酵素である[NiFe]ヒドロゲナーゼのモデルとなる化合物について、水素分子活性化機構解明の鍵となる水素原子の観察に成功しました。
天然の酵素である[NiFe]ヒドロゲナーゼは、水中・常温・常圧下で水素分子(H2)を、プロトン(H+)とヒドリドイオン(H−)又は、プロトン(H+)と電子(e−)へ変換します。この機能を解明し、水素エネルギー開発へ応用するという観点から、[NiFe]ヒドロゲナーゼの活性化状態の構造が注目されています。その候補として、図4-4で示すようにニッケル(Ni)と鉄(Fe)が水素で架橋された構造が提唱されてきました。しかし、このような構造を持つ化合物はこれまで未発見のため、ヒドロゲナーゼによる水素活性化機構は謎に包まれています。これに対し、九州大学の小江誠司教授のグループはFeの代わりに同族金属のルテニウム(Ru)を用いることで、[NiFe]ヒドロゲナーゼと類似の反応性を持つ化合物、すなわち[NiFe]ヒドロゲナーゼ活性中心モデル化合物の合成に成功しました(図4-5)。この化合物がNiとRuの間を水素原子が架橋した構造を持っているか否かは、[NiFe]ヒドロゲナーゼの活性構造を推定し、その酵素活性機構を解明する上で非常に重要です。しかし、通常の構造解析法であるX線回折は分子中の電子を観察するために電子を1個しか持たない水素原子の観察が難しく、この錯体の水素位置はこれまで確認できていませんでした。
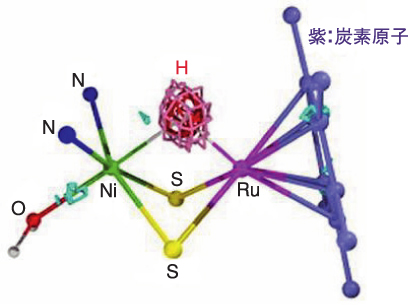
そこで私たちは、研究用原子炉JRR-3(Japan Research Reactor No.3)に設置した単結晶中性子回折計BIX-3を用いて、このモデル化合物の単結晶中性子構造解析を行いました。中性子は水素原子に対する感度が高く、散乱の特徴がほかの原子と大きく異なるため、水素原子を確実に観察できます。BIX-3回折計による測定では9日間で10,161個の回折点の強度を測定し、更に得られたデータから立体構造解析を行うことにより、NiとRuの間に水素原子が存在することを証明しました(図4-6)。こうして、この特殊な化合物はNiとRuの間を水素原子が架橋した構造を持つ世界初の化合物であることが証明され、天然の[NiFe]ヒドロゲナーゼでも同様の構造を経由して水素分子が活性化していることが示唆されました。
この成果は、新しい水素活性化触媒による水素エネルギー開発につながると期待されます。なお、本成果を含むヒドロゲナーゼモデル化合物の一連の研究は九州大学の小江教授のグループを中心として、独立行政法人科学技術振興機構(JST),大阪大学,兵庫県立大学,原子力機構の5機関の共同研究として行い、原子力機構は中性子による立体構造決定を担当しました。